इलेक्ट्रोलाइट म्हणजे काय
ज्या पदार्थांमध्ये विद्युत प्रवाह आयनांच्या हालचालीमुळे होतो, म्हणजे. आयनिक चालकतात्यांना इलेक्ट्रोलाइट्स म्हणतात. इलेक्ट्रोलाइट्स दुसर्या प्रकारच्या कंडक्टरशी संबंधित आहेत, कारण त्यातील विद्युत् प्रवाह रासायनिक प्रक्रियेशी संबंधित आहे, आणि केवळ धातूंप्रमाणेच इलेक्ट्रॉनच्या हालचालीशी संबंधित नाही.
द्रावणातील या पदार्थांचे रेणू इलेक्ट्रोलाइटिक पृथक्करण करण्यास सक्षम असतात, म्हणजेच ते सकारात्मक चार्ज केलेल्या (केशन्स) आणि नकारात्मक चार्ज केलेल्या (आयन) आयनमध्ये विरघळल्यावर विघटित होतात. घन इलेक्ट्रोलाइट्स, आयनिक वितळणे आणि इलेक्ट्रोलाइट द्रावण निसर्गात आढळू शकतात. सॉल्व्हेंटच्या प्रकारावर अवलंबून, इलेक्ट्रोलाइट्स जलीय आणि नॉन-जलीय असतात, तसेच एक विशेष प्रकार - पॉलीइलेक्ट्रोलाइट्स.
पाण्यात विरघळल्यावर ज्या आयनमध्ये पदार्थ विघटित होतो त्यावर अवलंबून, H + आणि OH- आयन नसलेले इलेक्ट्रोलाइट्स (मीठ इलेक्ट्रोलाइट्स), भरपूर प्रमाणात H + आयन (अॅसिड) असलेले इलेक्ट्रोलाइट्स आणि OH- आयनचे प्राबल्य असलेले इलेक्ट्रोलाइट्स ( बेस) वेगळे केले जाऊ शकते.
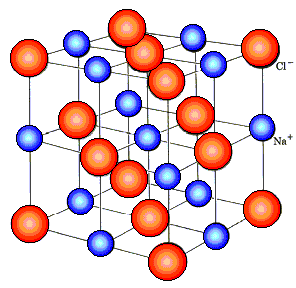
इलेक्ट्रोलाइट रेणूंच्या पृथक्करणादरम्यान समान संख्येने सकारात्मक आणि नकारात्मक आयन तयार झाल्यास, अशा इलेक्ट्रोलाइटला सममितीय म्हणतात.किंवा द्रावणातील सकारात्मक आणि ऋण आयनांची संख्या समान नसल्यास असममित. सममितीय इलेक्ट्रोलाइट्सची उदाहरणे - KCl - 1,1-व्हॅलेंट इलेक्ट्रोलाइट आणि CaSO4 - 2,2-व्हॅलेंट इलेक्ट्रोलाइट. असममित इलेक्ट्रोलाइटचा प्रतिनिधी आहे, उदाहरणार्थ, H2TAKA4 — एक 1,2-व्हॅलेंट इलेक्ट्रोलाइट.

सर्व इलेक्ट्रोलाइट्सचे पृथक्करण करण्याच्या क्षमतेनुसार, मजबूत आणि कमकुवत मध्ये विभागले जाऊ शकतात. सौम्य द्रावणातील मजबूत इलेक्ट्रोलाइट्स जवळजवळ पूर्णपणे आयनमध्ये विघटित होतात. यामध्ये मोठ्या प्रमाणात अजैविक क्षार, काही ऍसिडस् आणि जलीय द्रावणातील बेस किंवा अल्कोहोल, केटोन्स किंवा अमाइड्स सारख्या उच्च विघटन शक्तीसह सॉल्व्हेंट्सचा समावेश होतो.
कमकुवत इलेक्ट्रोलाइट्स केवळ अंशतः विघटित असतात आणि असंबद्ध रेणूंसह गतिमान समतोल असतात. यामध्ये मोठ्या प्रमाणात सेंद्रिय ऍसिडस् तसेच सॉल्व्हेंट्समधील अनेक बेस समाविष्ट आहेत.
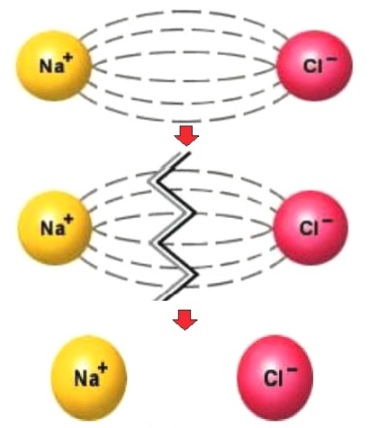
पृथक्करणाची डिग्री अनेक घटकांवर अवलंबून असते: तापमान, एकाग्रता आणि सॉल्व्हेंटचा प्रकार. तर, समान इलेक्ट्रोलाइट वेगवेगळ्या तापमानात, किंवा समान तापमानात परंतु वेगवेगळ्या सॉल्व्हेंट्समध्ये, वेगवेगळ्या अंशांमध्ये विलग केले जातील.
इलेक्ट्रोलाइटिक पृथक्करण, व्याख्येनुसार, द्रावणात मोठ्या संख्येने कण तयार करत असल्याने, यामुळे इलेक्ट्रोलाइट्स आणि विविध प्रकारच्या पदार्थांच्या द्रावणांच्या भौतिक गुणधर्मांमध्ये लक्षणीय फरक होतो: ऑस्मोटिक दाब वाढतो, द्रावणाच्या शुद्धतेच्या संबंधात गोठवणारे तापमान बदलते. आणि इतर.
इलेक्ट्रोलाइट आयन बहुतेक वेळा इलेक्ट्रोकेमिकल प्रक्रियांमध्ये आणि रासायनिक अभिक्रियांमध्ये स्वतंत्र गतिज एकके म्हणून भाग घेतात, द्रावणात उपस्थित असलेल्या इतर आयनांपेक्षा स्वतंत्र: इलेक्ट्रोलाइटमध्ये बुडलेल्या इलेक्ट्रोड्सवर, जेव्हा विद्युत् विद्युत् इलेक्ट्रोलाइटमधून जातो, तेव्हा ऑक्सिडेशन-कमी प्रतिक्रिया घडतात, ज्याची उत्पादने असतात. जे इलेक्ट्रोलाइट रचनेत जोडले जातात.
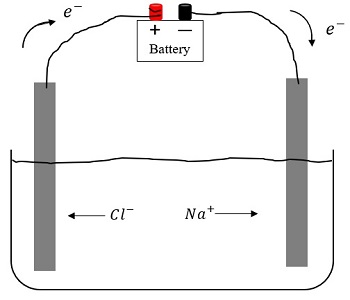
अशा प्रकारे, इलेक्ट्रोलाइट्स ही पदार्थांची जटिल प्रणाली आहे ज्यात आयन, विद्राव्य रेणू, असंबद्ध विद्राव्य रेणू, आयन जोड्या आणि मोठ्या संयुगे यांचा समावेश होतो. म्हणून, इलेक्ट्रोलाइट्सचे गुणधर्म अनेक घटकांद्वारे निर्धारित केले जातात: आयन-आण्विक आणि आयन-आयन परस्परसंवादाचे स्वरूप, विरघळलेल्या कणांच्या उपस्थितीत सॉल्व्हेंटच्या संरचनेत बदल इ.
ध्रुवीय इलेक्ट्रोलाइट्सचे आयन आणि रेणू एकमेकांशी खूप सक्रियपणे संवाद साधतात, ज्यामुळे सॉल्व्हेशन स्ट्रक्चर्स तयार होतात, ज्याची भूमिका आयनच्या आकारात घट आणि त्यांच्या व्हॅलेन्समध्ये वाढ झाल्यामुळे अधिक महत्त्वपूर्ण बनते. सॉल्व्हेशन एनर्जी हे इलेक्ट्रोलाइट आयन आणि सॉल्व्हेंट रेणूंच्या परस्परसंवादाचे मोजमाप आहे.
इलेक्ट्रोलाइट्स, त्यांच्या एकाग्रतेवर अवलंबून, आहेत: सौम्य समाधान, क्षणिक आणि केंद्रित. सौम्य द्रावणांची रचना शुद्ध विद्रावकासारखीच असते, परंतु उपस्थित आयन त्यांच्या प्रभावाने या संरचनेत व्यत्यय आणतात. आयनमधील इलेक्ट्रोस्टॅटिक परस्परसंवादामुळे मजबूत इलेक्ट्रोलाइट्सचे असे कमकुवत समाधान गुणधर्मांमधील आदर्श सोल्यूशन्सपेक्षा वेगळे असतात.
एकाग्रतेचा संक्रमण प्रदेश आयनांच्या प्रभावामुळे विलायकांच्या संरचनेत लक्षणीय बदल करून दर्शविला जातो.अगदी उच्च एकाग्रतेवर, बहुतेक दिवाळखोर रेणू आयनांसह विद्राव्य रचनांमध्ये भाग घेतात, त्यामुळे विद्रावकांची कमतरता निर्माण होते.
एकाग्र द्रावणाची रचना आयनिक वितळणे किंवा स्फटिकासारखे द्रावणाच्या जवळ असते, ज्याचे वैशिष्ट्य उच्च क्रमाने आणि आयनिक संरचनांची एकरूपता असते. या आयनिक संरचना जटिल परस्परसंवादाद्वारे एकमेकांशी आणि पाण्याच्या रेणूंशी जोडतात.
त्यांच्या गुणधर्मांचे उच्च-तापमान आणि कमी-तापमान प्रदेश, तसेच उच्च- आणि सामान्य-दाब क्षेत्र, इलेक्ट्रोलाइट्सचे वैशिष्ट्य आहेत. जसजसे दाब किंवा तापमान वाढते तसतसे द्रावणाचे दाढ क्रम कमी होते आणि द्रावणाच्या गुणधर्मांवर सहयोगी आणि सोलेशन प्रभावांचा प्रभाव कमकुवत होतो. आणि जेव्हा तापमान वितळण्याच्या बिंदूच्या खाली येते तेव्हा काही इलेक्ट्रोलाइट्स काचेच्या अवस्थेत जातात. अशा इलेक्ट्रोलाइटचे उदाहरण म्हणजे LiCl चे जलीय द्रावण.
आज, तंत्रज्ञान आणि जीवशास्त्राच्या जगात इलेक्ट्रोलाइट्स विशेषतः महत्त्वपूर्ण भूमिका बजावतात. जैविक प्रक्रियांमध्ये, इलेक्ट्रोलाइट्स अकार्बनिक आणि सेंद्रिय संश्लेषणासाठी एक माध्यम म्हणून आणि तंत्रज्ञानामध्ये इलेक्ट्रोकेमिकल उत्पादनासाठी आधार म्हणून कार्य करतात.
इलेक्ट्रोलिसिस, इलेक्ट्रोकॅटलिसिस, धातूंचे गंज, इलेक्ट्रोक्रिस्टलायझेशन - या घटना अनेक आधुनिक उद्योगांमध्ये, विशेषत: ऊर्जा आणि पर्यावरण संरक्षणाच्या दृष्टीने महत्त्वपूर्ण स्थान व्यापतात.
हे देखील पहा: पाण्याच्या इलेक्ट्रोलिसिसद्वारे हायड्रोजनचे उत्पादन - तंत्रज्ञान आणि उपकरणे



