बॅटरी कशा काम करतात आणि कार्य करतात
 तंत्रज्ञानातील शब्दाच्या व्यापक अर्थाने, "बॅटरी" हा शब्द अशा उपकरणास सूचित करतो जो विशिष्ट ऑपरेटिंग परिस्थितीत विशिष्ट प्रकारची ऊर्जा जमा करण्यास आणि इतरांना मानवी गरजांसाठी वापरण्याची परवानगी देतो.
तंत्रज्ञानातील शब्दाच्या व्यापक अर्थाने, "बॅटरी" हा शब्द अशा उपकरणास सूचित करतो जो विशिष्ट ऑपरेटिंग परिस्थितीत विशिष्ट प्रकारची ऊर्जा जमा करण्यास आणि इतरांना मानवी गरजांसाठी वापरण्याची परवानगी देतो.
ते वापरले जातात जेथे विशिष्ट वेळेसाठी ऊर्जा गोळा करणे आवश्यक असते आणि नंतर मोठ्या श्रम-केंद्रित प्रक्रिया पार पाडण्यासाठी त्याचा वापर केला जातो. उदाहरणार्थ, लॉकमध्ये वापरल्या जाणार्या हायड्रॉलिक संचयकांमुळे जहाजांना नदीच्या पात्रावर नवीन स्तरावर जाण्याची परवानगी मिळते.
इलेक्ट्रिक बॅटरी समान तत्त्वावर विजेसह कार्य करतात: प्रथम, ते बाह्य चार्जिंग स्त्रोताकडून वीज जमा करतात (संचय करतात) आणि नंतर कनेक्ट केलेल्या ग्राहकांना काम करण्यासाठी देतात. त्यांच्या स्वभावानुसार, ते स्त्राव आणि चार्जचे नियतकालिक चक्र पार पाडण्यास सक्षम असलेल्या रासायनिक वर्तमान स्त्रोतांशी संबंधित आहेत.
ऑपरेशन दरम्यान, इलेक्ट्रोड प्लेट्सच्या घटकांमध्ये त्यांच्या भरलेल्या पदार्थ - इलेक्ट्रोलाइटसह रासायनिक प्रतिक्रिया सतत घडत असतात.
जेव्हा विद्युतीय संपर्क प्रदान करण्यासाठी जहाजाच्या मुख्य भागामध्ये तारांसह वेगवेगळ्या धातूंच्या दोन प्लेट्स घातल्या जातात तेव्हा बॅटरी उपकरणाचा योजनाबद्ध आकृती सरलीकृत रेखाचित्राद्वारे दर्शविला जाऊ शकतो. प्लेट्स दरम्यान इलेक्ट्रोलाइट ओतला जातो.
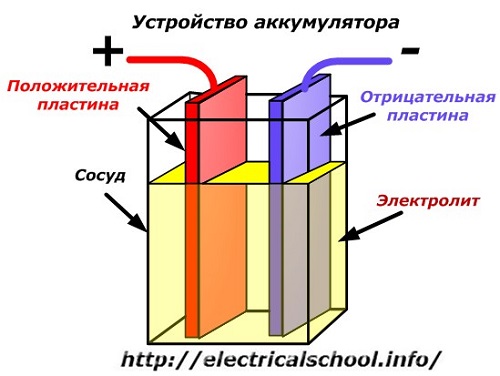
डिस्चार्ज केल्यावर बॅटरी ऑपरेशन
जेव्हा एखादा भार, जसे की लाइट बल्ब, इलेक्ट्रोडशी जोडलेले असते, तेव्हा एक बंद इलेक्ट्रिकल सर्किट तयार होते ज्याद्वारे डिस्चार्ज करंट वाहतो. हे धातूच्या भागांमधील इलेक्ट्रॉन्स आणि इलेक्ट्रोलाइटमधील केशन्ससह आयनच्या हालचालींद्वारे तयार होते.
ही प्रक्रिया पारंपारिकपणे निकेल-कॅडमियम इलेक्ट्रोड डिझाइनसह आकृतीवर दर्शविली जाते.
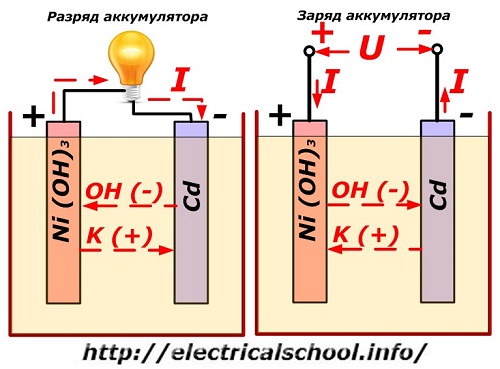
येथे, ग्रेफाइट ऍडिटीव्हसह निकेल ऑक्साईड्स, जे विद्युत चालकता वाढवतात, सकारात्मक इलेक्ट्रोडची सामग्री म्हणून वापरली जातात. नकारात्मक इलेक्ट्रोडचा धातू स्पंज कॅडमियम आहे.
डिस्चार्ज दरम्यान, निकेल ऑक्साईडचे सक्रिय ऑक्सिजन कण इलेक्ट्रोलाइटमध्ये सोडले जातात आणि नकारात्मक प्लेट्सकडे निर्देशित केले जातात, जेथे कॅडमियमचे ऑक्सीकरण होते.
चार्ज करताना बॅटरीची कार्यक्षमता
जेव्हा लोड बंद केले जाते, तेव्हा समान ध्रुवीयतेच्या चार्ज केलेल्या बॅटरीपेक्षा जास्त मूल्याच्या प्लेट टर्मिनल्सवर स्थिर (विशिष्ट परिस्थितींमध्ये, स्पंदन करणारा) व्होल्टेज लागू केला जातो, जेव्हा स्त्रोत आणि ग्राहकांचे प्लस आणि मायनस टर्मिनल्स एकरूप होतात. .
चार्जरमध्ये नेहमी अधिक शक्ती असते, जी बॅटरीमधील अवशिष्ट ऊर्जा "दडपून टाकते" आणि डिस्चार्जच्या विरुद्ध दिशेने विद्युत प्रवाह तयार करते. परिणामी, इलेक्ट्रोड आणि इलेक्ट्रोलाइटमधील अंतर्गत रासायनिक प्रक्रिया बदलतात. उदाहरणार्थ, निकेल-कॅडमियम प्लेट्सच्या बॉक्सवर, सकारात्मक इलेक्ट्रोड ऑक्सिजनसह समृद्ध होतो आणि नकारात्मक - शुद्ध कॅडमियमच्या स्थितीत.
जेव्हा बॅटरी डिस्चार्ज केली जाते आणि चार्ज केली जाते तेव्हा प्लेट्सच्या (इलेक्ट्रोड्स) सामग्रीची रासायनिक रचना बदलते, परंतु इलेक्ट्रोलाइट बदलत नाही.
बॅटरी कनेक्शन पद्धती
समांतर कनेक्शन
एखादी व्यक्ती किती डिस्चार्ज वर्तमान सहन करू शकते हे अनेक घटकांवर अवलंबून असते, परंतु प्रामुख्याने डिझाइन, वापरलेली सामग्री आणि त्यांचे परिमाण. इलेक्ट्रोड्सवरील प्लेट्सचे क्षेत्रफळ जितके मोठे असेल तितके जास्त विद्युत् प्रवाह ते सहन करू शकतात.
हे तत्त्व समान प्रकारच्या पेशींना बॅटरीमध्ये समांतर जोडण्यासाठी वापरले जाते जेव्हा विद्युत प्रवाह लोडमध्ये वाढवणे आवश्यक असते. परंतु अशा डिझाइनला चार्ज करण्यासाठी, स्त्रोताची शक्ती वाढवणे आवश्यक असेल. ही पद्धत क्वचितच तयार संरचनांसाठी वापरली जाते, कारण आता आवश्यक बॅटरी त्वरित खरेदी करणे खूप सोपे आहे. परंतु ऍसिड बॅटरी उत्पादक ते वापरतात, वेगवेगळ्या प्लेट्सला सिंगल ब्लॉक्समध्ये जोडतात.
सीरियल कनेक्शन
वापरलेल्या सामग्रीवर अवलंबून, दैनंदिन जीवनात सामान्य असलेल्या बॅटरीच्या दोन इलेक्ट्रोड प्लेट्समध्ये 1.2 / 1.5 किंवा 2.0 व्होल्टचा व्होल्टेज तयार केला जाऊ शकतो. (वास्तविक, ही श्रेणी खूपच विस्तृत आहे.) अर्थातच, अनेक विद्युत उपकरणांसाठी ते पुरेसे नाही. म्हणून, समान प्रकारच्या बॅटरी मालिकेत जोडल्या जातात आणि हे बर्याचदा एका प्रकरणात केले जाते.
अशा डिझाइनचे उदाहरण म्हणजे सल्फ्यूरिक ऍसिड आणि लीड इलेक्ट्रोड प्लेट्सवर आधारित व्यापक ऑटोमोटिव्ह विकास.
सहसा, लोकांमध्ये, विशेषत: वाहतूक चालकांमध्ये, कोणत्याही डिव्हाइसला बॅटरी म्हणण्याची प्रथा आहे, त्याच्या घटक घटकांची संख्या विचारात न घेता - बॉक्स. तथापि, हे पूर्णपणे योग्य नाही.मालिकेत जोडलेल्या अनेक बॉक्सेसमधून एकत्र केलेली रचना ही आधीपासूनच बॅटरी आहे, ज्यासाठी संक्षिप्त नाव «АКБ» चिकटवले आहे... तिची अंतर्गत रचना आकृतीमध्ये दर्शविली आहे.
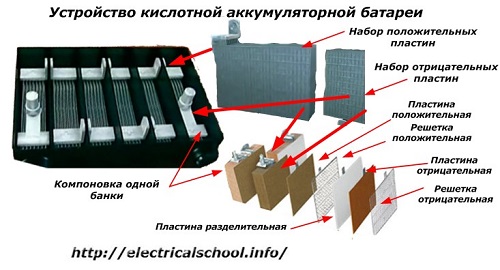
प्रत्येक जारमध्ये सकारात्मक आणि नकारात्मक इलेक्ट्रोडसाठी प्लेट्सच्या संचासह दोन ब्लॉक्स असतात. इलेक्ट्रोलाइटद्वारे विश्वसनीय गॅल्व्हॅनिक कनेक्शनच्या शक्यतेसह धातूच्या संपर्काशिवाय ब्लॉक्स एकमेकांमध्ये बसतात.
या प्रकरणात, संपर्क प्लेट्समध्ये अतिरिक्त ग्रिड असते आणि विभाजक प्लेटद्वारे एकमेकांपासून वेगळे केले जाते.
ब्लॉक्समध्ये प्लेट्स कनेक्ट केल्याने त्यांचे कार्य क्षेत्र वाढते, संपूर्ण संरचनेचा एकूण प्रतिकार कमी होतो आणि आपल्याला कनेक्ट केलेल्या लोडची शक्ती वाढविण्यास अनुमती देते.
बॉक्सच्या बाहेरील बाजूस, अशा बॅटरीमध्ये खालील आकृतीमध्ये दर्शविलेले घटक आहेत.
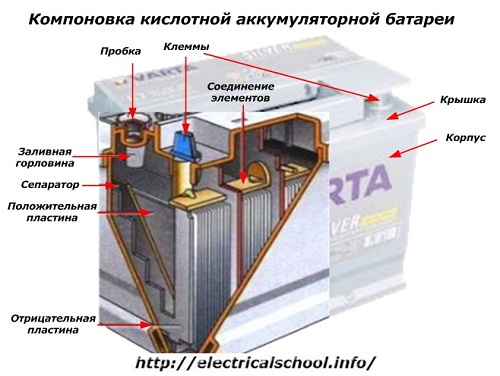
हे दर्शविते की बळकट प्लॅस्टिक घरे कव्हरने सील केलेले आहेत आणि कारच्या इलेक्ट्रिकल सर्किटशी कनेक्शनसाठी दोन टर्मिनल्स (सामान्यतः शंकूच्या आकाराचे) सह सुसज्ज आहेत. ध्रुवीयता खुणा त्यांच्या टर्मिनल्सवर मुद्रांकित केल्या जातात: «+» आणि «-«. वायरिंग त्रुटींना अवरोधित करण्यासाठी सामान्यतः सकारात्मक टर्मिनलचा व्यास नकारात्मक टर्मिनलपेक्षा थोडा मोठा असतो.
इलेक्ट्रोलाइट पातळी नियंत्रित करण्यासाठी किंवा ऑपरेशन दरम्यान डिस्टिल्ड वॉटर जोडण्यासाठी सेवायोग्य बॅटरीमध्ये प्रत्येक जारच्या वर एक फिलर होल असतो. त्यामध्ये एक प्लग स्क्रू केला जातो, जो केसच्या अंतर्गत पोकळ्यांना दूषित होण्यापासून वाचवतो आणि त्याच वेळी जेव्हा बॅटरी झुकलेली असते तेव्हा इलेक्ट्रोलाइटला गळती होण्यापासून प्रतिबंधित करते.
शक्तिशाली चार्जसह, इलेक्ट्रोलाइटमधून गॅसिंग शक्य आहे (आणि ही प्रक्रिया गहन ड्रायव्हिंग दरम्यान शक्य आहे), बॉक्सच्या आत दबाव वाढू नये म्हणून प्लगमध्ये छिद्र केले जातात.ऑक्सिजन आणि हायड्रोजन, तसेच इलेक्ट्रोलाइट वाष्प त्यांच्यामधून बाहेर पडतात. अत्याधिक चार्जिंग करंट्सचा समावेश असलेल्या अशा परिस्थिती टाळण्याची शिफारस केली जाते.
समान आकृती बँकांमधील घटकांचे कनेक्शन आणि इलेक्ट्रोड प्लेट्सची व्यवस्था दर्शवते.
कार स्टार्टर बॅटरी (लीड ऍसिड) डबल सल्फेशनच्या तत्त्वावर कार्य करतात. डिस्चार्ज / चार्जिंग दरम्यान, इलेक्ट्रोलाइट (सल्फ्यूरिक ऍसिड) मध्ये पाणी सोडणे / शोषून घेण्यासह इलेक्ट्रोडच्या सक्रिय वस्तुमानाच्या रासायनिक रचनेत बदलांसह, त्यांच्यावर एक इलेक्ट्रोकेमिकल प्रक्रिया होते.
हे चार्जिंग करताना इलेक्ट्रोलाइटच्या विशिष्ट गुरुत्वाकर्षणात वाढ आणि बॅटरी डिस्चार्ज झाल्यावर कमी झाल्याचे स्पष्ट करते. दुसऱ्या शब्दांत, घनता मूल्य आपल्याला बॅटरीच्या विद्युतीय स्थितीचे मूल्यांकन करण्यास अनुमती देते. ते मोजण्यासाठी एक विशेष उपकरण वापरले जाते - एक कार हायड्रोमीटर.
डिस्टिल्ड वॉटर, जे ऍसिड बॅटरीच्या इलेक्ट्रोलाइटचा भाग आहे, घन स्थितीत बदलते - नकारात्मक तापमानात बर्फ. म्हणून, थंड हवामानात कारच्या बॅटरी गोठण्यापासून रोखण्यासाठी, नियमांमध्ये प्रदान केलेल्या विशेष उपाययोजना लागू करणे आवश्यक आहे. शोषणासाठी.
कोणत्या प्रकारच्या बॅटरी आहेत?
विविध उद्देशांसाठी आधुनिक उत्पादन इलेक्ट्रोड आणि इलेक्ट्रोलाइटच्या वेगवेगळ्या रचनांसह तीन डझनपेक्षा जास्त उत्पादने तयार करतात. 12 ज्ञात मॉडेल फक्त लिथियमवर चालतात.

इलेक्ट्रोड मेटल म्हणून खालील आढळू शकतात:
-
आघाडी
-
लोखंड
-
लिथियम;
-
टायटॅनियम;
-
कोबाल्ट;
-
कॅडमियम;
-
निकेल;
-
जस्त;
-
चांदी;
-
व्हॅनिडियम;
-
अॅल्युमिनियम
-
काही इतर वस्तू.
ते इलेक्ट्रिकल आउटपुट वैशिष्ट्यांवर आणि म्हणून अनुप्रयोगावर परिणाम करतात.
इलेक्ट्रिक स्टार्टर मोटर्सद्वारे अंतर्गत ज्वलन इंजिनच्या क्रँकशाफ्टच्या फिरण्यामुळे निर्माण होणारा अल्पकालीन उच्च भार सहन करण्याची क्षमता हे लीड-ऍसिड बॅटरीचे वैशिष्ट्य आहे. ते वाहतूक, अखंडित वीज पुरवठा आणि आपत्कालीन उर्जा प्रणालींमध्ये मोठ्या प्रमाणावर वापरले जातात.
मानक गॅल्व्हॅनिक पेशी (नियमित बॅटरी) सामान्यतः निकेल-कॅडमियम, निकेल-जस्त आणि निकेल-मेटल हायड्राइड बॅटरीद्वारे बदलल्या जातात.
परंतु लिथियम-आयन किंवा लिथियम-पॉलिमर डिझाइन मोबाइल आणि संगणकीय उपकरणे, बांधकाम साधने आणि अगदी इलेक्ट्रिक वाहनांमध्ये विश्वसनीयपणे कार्य करतात.
वापरलेल्या इलेक्ट्रोलाइटच्या प्रकारानुसार, बॅटरी आहेत:
-
आंबट
-
अल्कधर्मी
उद्देशानुसार बॅटरीचे वर्गीकरण आहे. उदाहरणार्थ, आधुनिक परिस्थितीत, उपकरणे दिसू लागली आहेत जी ऊर्जा हस्तांतरणासाठी वापरली जातात - इतर स्त्रोतांचे रिचार्जिंग. तथाकथित बाह्य बॅटरी अनेक मोबाइल उपकरणांच्या मालकांना पर्यायी विद्युत नेटवर्कच्या अनुपस्थितीत मदत करते. हे टॅब्लेट, स्मार्टफोन, मोबाइल फोन वारंवार चार्ज करण्यास सक्षम आहे.
या सर्व बॅटरीमध्ये ऑपरेशनचे समान तत्त्व आणि एक समान उपकरण आहे. उदाहरणार्थ, खालील आकृतीमध्ये दर्शविलेले लिथियम-आयन फिंगर मॉडेल अनेक प्रकारे आधी चर्चा केलेल्या ऍसिड बॅटरीच्या डिझाइनची पुनरावृत्ती करते.
येथे आपण समान संपर्क इलेक्ट्रोड, प्लेट्स, विभाजक आणि गृहनिर्माण पाहतो. फक्त ते इतर कामकाजाच्या परिस्थिती लक्षात घेऊन तयार केले जातात.
बॅटरीची मूलभूत विद्युत वैशिष्ट्ये
डिव्हाइसचे ऑपरेशन पॅरामीटर्सद्वारे प्रभावित होते:
-
क्षमता;
-
ऊर्जा घनता;
-
स्वत: ची स्त्राव;
-
तापमान व्यवस्था.
क्षमतेला बॅटरीचा जास्तीत जास्त चार्ज म्हणतात, जो डिस्चार्ज दरम्यान सर्वात कमी व्होल्टेजला देण्यास सक्षम आहे. हे पेंडेंट (एसआय सिस्टम) आणि अँपिअर-तास (नॉन-सिस्टम युनिट) मध्ये व्यक्त केले जाते.
क्षमतेचा एक प्रकार म्हणून "ऊर्जा क्षमता" असते, जी डिस्चार्ज दरम्यान सोडलेली ऊर्जा किमान स्वीकार्य व्होल्टेजपर्यंत निर्धारित करते. हे जूल (SI) आणि वॅट-तास (नॉन-SI युनिट) मध्ये मोजले जाते.
उर्जेची घनता बॅटरीचे वजन किंवा व्हॉल्यूम आणि उर्जेच्या प्रमाणाचे गुणोत्तर म्हणून व्यक्त केली जाते.
सेल्फ-डिस्चार्ज टर्मिनल्सवर लोड नसताना चार्जिंगनंतर क्षमतेचे नुकसान विचारात घ्या. हे डिझाइनवर अवलंबून असते आणि अनेक कारणांमुळे इलेक्ट्रोडमधील इन्सुलेशन ब्रेकडाउनमुळे वाढते.
ऑपरेटिंग तापमान विद्युत गुणधर्मांवर परिणाम करते आणि निर्मात्याने निर्दिष्ट केलेल्या मानकांपासून गंभीर विचलन झाल्यास, ते बॅटरीचे नुकसान करू शकते. उष्णता आणि सर्दी अस्वीकार्य आहेत, ते रासायनिक अभिक्रिया आणि बॉक्सच्या आत असलेल्या वातावरणाच्या दबावावर परिणाम करतात.
