संपर्क क्षमता मध्ये फरक
जर दोन भिन्न धातूंचे दोन नमुने एकत्र घट्ट दाबले गेले तर त्यांच्यामध्ये संपर्क संभाव्य फरक निर्माण होईल. इटालियन भौतिकशास्त्रज्ञ, रसायनशास्त्रज्ञ आणि फिजियोलॉजिस्ट अॅलेसॅन्ड्रो व्होल्टा यांनी 1797 मध्ये धातूंच्या विद्युत गुणधर्मांचा अभ्यास करताना ही घटना शोधली.

मग व्होल्टाला आढळले की जर तुम्ही धातूंना या क्रमाने साखळीत जोडले: Al, Zn, Sn, Pb, Bi, Hg, Fe, Cu, Ag, Au, Pt, Pd, तर परिणामी साखळीतील प्रत्येक पुढील धातू प्राप्त होईल. ची संभाव्यता - मागीलपेक्षा कमी. शिवाय, शास्त्रज्ञाला असे आढळून आले की अशा प्रकारे अनेक धातू एकत्रित केल्यामुळे तयार झालेल्या सर्किटच्या टोकांमध्ये समान संभाव्य फरक मिळेल, या सर्किटमधील या धातूंच्या व्यवस्थेचा क्रम विचारात न घेता - ही स्थिती आता व्होल्टाचा मालिका संपर्क नियम म्हणून ओळखली जाते. .
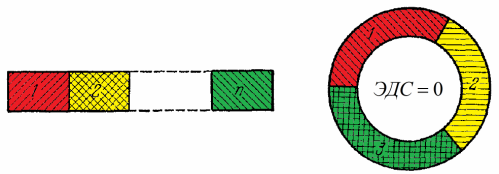
येथे हे समजून घेणे अत्यंत महत्वाचे आहे की संपर्क क्रमाच्या कायद्याच्या अचूक अंमलबजावणीसाठी, संपूर्ण मेटल सर्किट समान तापमानात असणे आवश्यक आहे.
जर हे सर्किट आता स्वतःच्या टोकापासून बंद केले असेल, तर ते सर्किटमधील EMF शून्य असेल या कायद्याचे पालन करते.परंतु जर हे सर्व (धातू 1, धातू 2, धातू 3) समान तापमानात असतील तरच, अन्यथा निसर्गाच्या मूलभूत नियमाचे-ऊर्जेच्या संवर्धनाच्या नियमाचे उल्लंघन होईल.
वेगवेगळ्या धातूंच्या जोड्यांसाठी, संपर्क संभाव्य फरक स्वतःचा असेल, व्होल्टच्या दहाव्या आणि शंभरावा भागापासून ते काही व्होल्टपर्यंत.
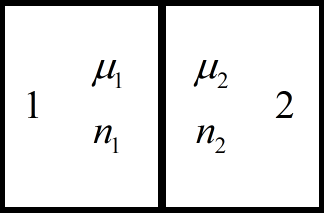
संपर्क संभाव्य फरक दिसण्याचे कारण समजून घेण्यासाठी, विनामूल्य इलेक्ट्रॉन मॉडेल वापरणे सोयीचे आहे.
जोडीतील दोन्ही धातू निरपेक्ष शून्य तपमानावर असू द्या, नंतर फर्मी मर्यादेसह सर्व ऊर्जा पातळी इलेक्ट्रॉनने भरल्या जातील. फर्मी उर्जेचे मूल्य (मर्यादा) खालीलप्रमाणे धातूमधील वहन इलेक्ट्रॉनच्या एकाग्रतेशी संबंधित आहे:
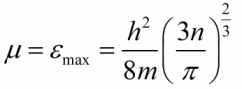
m हे इलेक्ट्रॉनचे उर्वरित वस्तुमान आहे, h हा प्लँकचा स्थिरांक आहे, n म्हणजे वहन इलेक्ट्रॉनची एकाग्रता
हे गुणोत्तर विचारात घेऊन, आम्ही वेगवेगळ्या फर्मी उर्जेसह आणि त्यामुळे वहन इलेक्ट्रॉनच्या भिन्न एकाग्रतेसह दोन धातूंचा जवळचा संपर्क आणतो.
आपल्या उदाहरणासाठी असे गृहीत धरू की दुसऱ्या धातूमध्ये वहन इलेक्ट्रॉनचे प्रमाण जास्त आहे आणि त्यानुसार दुसऱ्या धातूची फर्मी पातळी पहिल्या धातूपेक्षा जास्त आहे.
नंतर, जेव्हा धातू एकमेकांच्या संपर्कात येतात, तेव्हा इलेक्ट्रॉनचा प्रसार (एका धातूपासून दुसऱ्या धातूमध्ये प्रवेश) धातू 2 ते धातू 1 पर्यंत सुरू होईल, कारण धातू 2 ने ऊर्जा पातळी भरली आहे जी पहिल्या धातूच्या फर्मी पातळीपेक्षा जास्त आहे. , ज्याचा अर्थ असा आहे की या स्तरांवरील इलेक्ट्रॉन मेटल 1 रिक्त जागा भरतील.
अशा परिस्थितीत इलेक्ट्रॉनची उलट हालचाल उत्साहीपणे अशक्य आहे, कारण दुसऱ्या धातूमध्ये सर्व खालच्या ऊर्जा पातळी आधीच पूर्णपणे भरल्या आहेत.अखेरीस, धातू 2 सकारात्मक चार्ज होईल आणि धातू 1 नकारात्मक चार्ज होईल, तर पहिल्या धातूची फर्मी पातळी पूर्वीपेक्षा जास्त होईल आणि दुसऱ्या धातूची कमी होईल. हा बदल पुढीलप्रमाणे असेल.
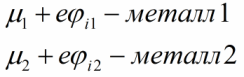
परिणामी, संपर्क साधणारे धातू आणि संबंधित विद्युत क्षेत्र यांच्यात संभाव्य फरक निर्माण होईल, जो आता इलेक्ट्रॉनच्या पुढील प्रसारास प्रतिबंध करेल.
जेव्हा संभाव्य फरक दोन धातूंच्या फर्मी स्तरांच्या समानतेशी संबंधित विशिष्ट मूल्यापर्यंत पोहोचतो तेव्हा त्याची प्रक्रिया पूर्णपणे थांबते, ज्यामध्ये धातू 2 मधून नव्याने आलेल्या इलेक्ट्रॉनसाठी धातू 1 मध्ये आणि धातू 2 मध्ये कोणतेही मुक्त स्तर नसतात. धातू 1 पासून इलेक्ट्रॉन स्थलांतराच्या शक्यतेवर कोणतेही स्तर मुक्त केले जाणार नाहीत. ऊर्जा संतुलन येईल:

इलेक्ट्रॉनचा चार्ज ऋणात्मक असल्याने, पोटेंशिअलच्या सापेक्ष आपली खालील स्थिती असेल:

जरी आपण मूलतः धातूंचे तापमान निरपेक्ष शून्य आहे असे गृहीत धरले असले, तरी त्याच पद्धतीने कोणत्याही तापमानात समतोल निर्माण होईल.
विद्युत क्षेत्राच्या उपस्थितीत फर्मी उर्जा ही त्या एका इलेक्ट्रॉनच्या चार्जला संदर्भित केलेल्या इलेक्ट्रॉन गॅसमधील एका इलेक्ट्रॉनच्या रासायनिक संभाव्यतेपेक्षा अधिक काही नसते आणि समतोल स्थितीत दोन्ही धातूंच्या इलेक्ट्रॉन वायूंच्या रासायनिक संभाव्यतेपेक्षा समान असेल, फक्त तापमानावरील रासायनिक संभाव्यतेचे अवलंबन विचारात जोडणे आवश्यक आहे.
म्हणून, आमच्याद्वारे विचारात घेतलेल्या संभाव्य फरकाला अंतर्गत संपर्क संभाव्य फरक म्हणतात आणि मालिका संपर्कांसाठी व्होल्टाच्या नियमाशी संबंधित आहे.
या संभाव्य फरकाचा अंदाज लावू या, यासाठी आपण फर्मी ऊर्जा प्रवाहकीय इलेक्ट्रॉनच्या एकाग्रतेच्या संदर्भात व्यक्त करतो, त्यानंतर स्थिरांकांची संख्यात्मक मूल्ये बदलतो:
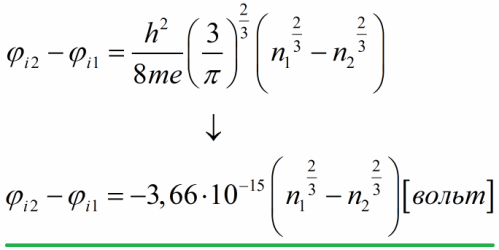
अशा प्रकारे, मुक्त इलेक्ट्रॉन मॉडेलच्या आधारे, धातूंसाठी अंतर्गत संपर्क संभाव्य फरक एका व्होल्टच्या शंभरव्या भागापासून अनेक व्होल्टपर्यंतच्या परिमाणाच्या क्रमानुसार असतो.
